Explicamos o que é a separação de misturas e os métodos que ela usa. Além disso, quais são suas características gerais e os tipos de misturas.

Qual é a separação de misturas?
A separação de misturas ou separação de fases é um processo físico pelo qual os componentes de uma mistura podem ser separados . Esses componentes não mudam durante o processo de separação, mas permanecem os mesmos, apenas que após a separação os componentes se separaram.
A separação de misturas é um processo físico, não químico . Isso significa que novas substâncias não se constituem após a separação das misturas, como acontece nos processos químicos, onde duas ou mais substâncias são combinadas quimicamente (quebradas e formadas ligações químicas ) para formar novas.
Existem diferentes métodos, incluindo filtração, decantação, destilação, evaporação, centrifugação, levigação, magnetização, lixiviação seletiva, flotação e cristalização, entre outros. A escolha do método de separação dependerá do tipo de mistura a ser separada, visto que existem misturas homogêneas e misturas heterogêneas.
Veja também: Fluidos
Finalidades da separação de misturas

As separações das misturas têm diferentes finalidades ou objetivos :
- Use os componentes de uma mistura (homogênea ou heterogênea) individualmente em outros processos.
- Quantifique separadamente as substâncias que os compõem.
- Realize combinações dos diferentes métodos de separação para melhorar ou facilitar a separação de misturas complexas ou difíceis de separar.
Fases de uma mistura

Existem pelo menos duas fases que compõem as misturas:
- Fase dispersa . É a fase que se encontra em menor proporção na mistura. Pode ser composto por uma ou mais substâncias que se dispersam ou se dissolvem em outra (fase de dispersão). Por exemplo, em uma solução de sal em água, o sal é a fase dispersa ou dissolvida, enquanto a água é a fase de dispersão.
- Fase de dispersão . É a fase que se encontra em maior proporção na mistura. Uma ou mais fases podem ser dispersas ou dissolvidas nele (fase dispersa). No exemplo anterior, a fase de dispersão seria a água, por >sal ).
Tipos de mistura
Existem dois tipos de misturas:
- Misturas homogêneas . Eles se caracterizam por não ser possível distinguir suas fases a olho nu (mesmo ao microscópio ). As mais comuns são as misturas de sólidos com sólidos ou de líquidos com líquidos . Por exemplo: água sanitária (que pode conter diferentes quantidades de cloro), café com leite, açúcar em água , limonada, tintura de iodo, entre outros. Eles são conhecidos como soluções.
- Misturas heterogêneas . Essas misturas apresentam descontinuidades, ou seja, é possível distinguir suas diferentes fases. Alguns exemplos de misturas heterogêneas são cimento, água do mar , areia em água, água e óleo, óleo e vinagre. Por sua vez, eles podem ser divididos em:
- Misturas simples ou grosseiras . Os componentes podem ser distinguidos ou diferenciados a olho nu. Por exemplo, uma salada de alface e tomate.
- Suspensões . As partículas das substâncias sólidas são minúsculas e não podem ser reconhecidas a olho nu, mas quando a mistura fica em repouso por um certo tempo, é possível distingui-las no fundo do recipiente, à medida que descem pelo líquido. Por exemplo, uma mistura de água e talco.
Exemplos de misturas na vida cotidiana
Em nossas vidas estamos continuamente em contato com diferentes misturas, sejam elas homogêneas ou heterogêneas. Por exemplo:
- A água do mar é uma mistura de cloreto de sódio (NaCl), água e outros componentes.
- O concreto ou concreto, usado na construção, é uma mistura de cimento, água, areia e cascalho.
- Um latte, o alimento básico do café da manhã da maioria das pessoas, é uma mistura.
- O bronze é uma mistura de cobre e estanho chamada liga.
Diferença entre mistura e reação química

Uma mistura é a combinação de duas ou mais substâncias , mas essa combinação não envolve a formação de uma ou mais novas substâncias, como ocorre em uma reação química. Em uma mistura, as substâncias misturadas mantêm suas propriedades químicas e composição química inalteradas.
Por outro lado, em uma reação química, as substâncias reagentes podem quebrar suas ligações químicas para se recombinar de outra forma com outras substâncias (que também quebram suas ligações) e, assim, formar novas ligações, o que implica a formação de novos compostos químicos.
Diferença entre mistura e composto químico
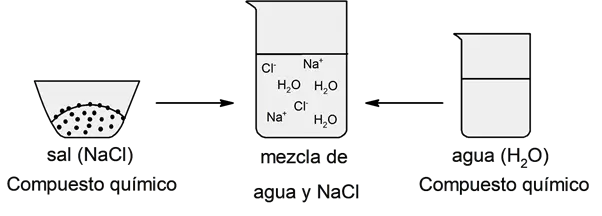
Os componentes de uma mistura podem ser separados usando métodos de separação física , enquanto os elementos que formam um composto químico não podem ser separados por estes métodos: para isso, métodos de separação química são necessários.
A razão para isso é que nas misturas os componentes não formam ligações químicas, enquanto os elementos formam ligações químicas para formar um determinado composto químico. Além disso, nos compostos químicos esses elementos estão ligados em proporções definidas, o que permite que sejam representados por fórmulas químicas, enquanto as misturas não podem ser representadas dessa forma.
Propriedades físicas de misturas
As propriedades físicas das misturas, como ponto de ebulição ou congelamento , podem ser diferentes daquelas de seus componentes individuais.
Por exemplo, quando o sal de cozinha é adicionado à água (quando contém essa substância dissolvida), o ponto de ebulição da mistura aumenta e o ponto de congelamento diminui, em comparação com a água pura. A primeira é chamada de aumento ebuloscópico e a segunda descida crioscópica.
Alguns métodos de separação de misturas
Os métodos de separação de misturas são métodos físicos baseados em alguma propriedade física dos componentes da mistura a ser separada, como ponto de fusão, ponto de ebulição, estado de agregação, magnetismo, entre outras.
- Filtração . É usado para separar um sólido de um líquido, desde que o sólido seja insolúvel no líquido. É utilizado um filtro por onde passa a mistura, o sólido é retido no filtro e o líquido passa por ele.

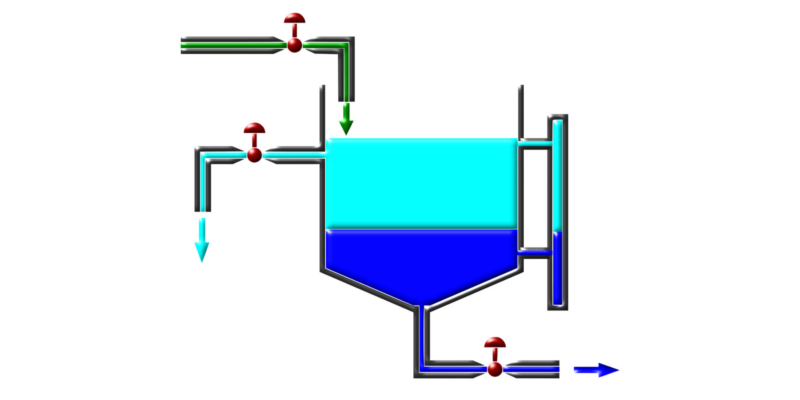
- Decantação. É usado para separar misturas de dois líquidos insolúveis um do outro ou misturas de um sólido e um líquido, também insolúveis um no outro. Para conseguir a separação, a mistura é deixada em um funil separador, a substância mais densa descerá, enquanto a menos densa ficará na superfície. Em seguida, a torneira do funil é aberta e a substância mais densa pode passar.
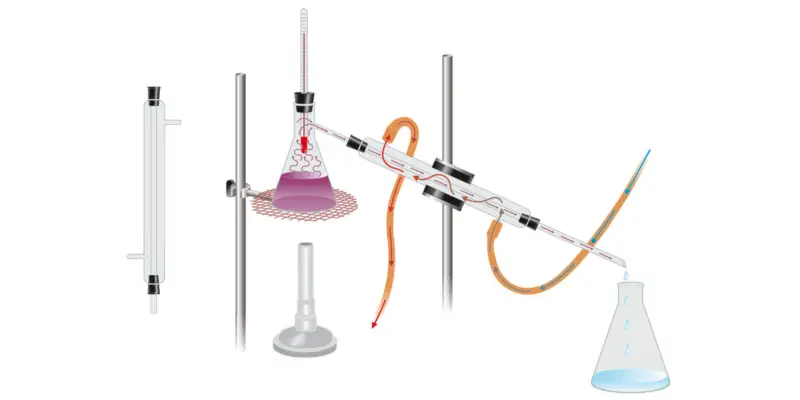
- Destilação . Este método serve para separar misturas de líquidos que são solúveis uns nos outros. Baseia-se nas diferenças de pontos de ebulição de diferentes líquidos. Para separar a mistura, primeiro é aplicado calor a ela até que o líquido com ponto de ebulição inferior passe para a fase de vapor e seja condensado em outro recipiente. Desta forma, é separado do líquido com maior ponto de ebulição, que fica apenas no recipiente onde se encontrava originalmente a mistura.
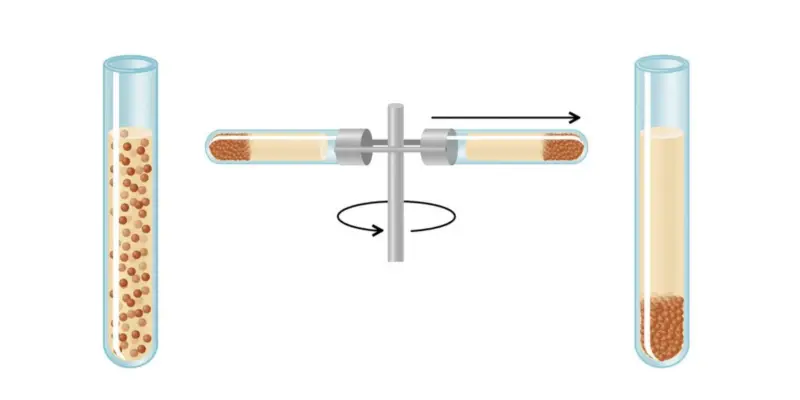
- Centrifugação . Geralmente é usado para separar um sólido insolúvel de um líquido. A mistura é centrifugada (um recipiente giratório), fazendo com que a força centrífuga envie o sólido para o fundo do recipiente e deixe o líquido no topo. Eles podem então ser separados por decantação.
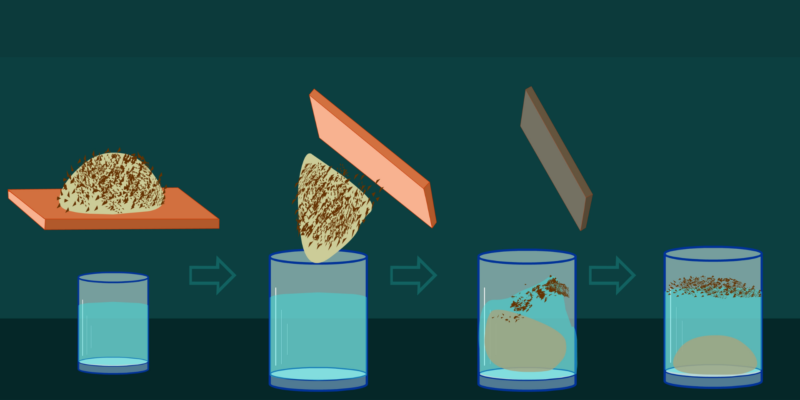
- Levigação . É usado para separar misturas de sólidos. Os sólidos são triturados e um solvente é adicionado. Então, essa nova mistura pode ser separada de acordo com as diferentes densidades de seus componentes.
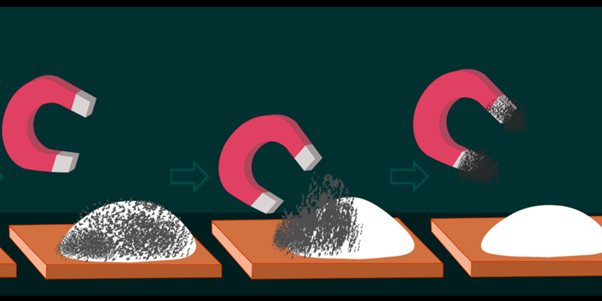
- Imantação . Consiste em separar uma mistura de substâncias em que pelo menos uma delas possui propriedades magnéticas e pode ser atraída por um ímã.
- Lixiviação seletiva . É um método que usa diferentes solventes para separar uma mistura. Cada componente da mistura terá uma afinidade maior por um solvente específico, portanto, quando cada solvente for colocado em contato com a mistura, será separado o componente que estiver mais relacionado a ele. Este processo é amplamente utilizado na mineração para extrair ouro .

Pode te ajudar: Coloides