Explicamos o que é ácido acético, como é sua fórmula e as propriedades que apresenta. Além disso, suas características, usos e exemplos.

O que é ácido acético?
Ácido acético, ácido methylcarboxylic ou também ácido etanóico é um composto orgânico que pode ser encontrado como um ião acetato ou etanoato ([C 2 H 3 O 2 ] – ) . Está presente no vinagre, um líquido que lhe confere cheiro e sabor azedo característicos.
É um ácido fraco, resultado comum em certos processos de fermentação , como os que ocorrem no vinho ou na fruta. É amplamente utilizado em aplicações de química orgânica e em vários processos industriais.
Sua produção massiva no mundo se deve ao fato de ser um composto útil na obtenção de outras substâncias orgânicas , como o ácido acrílico.
Veja também: ácido sulfúrico
Fórmula de ácido acético
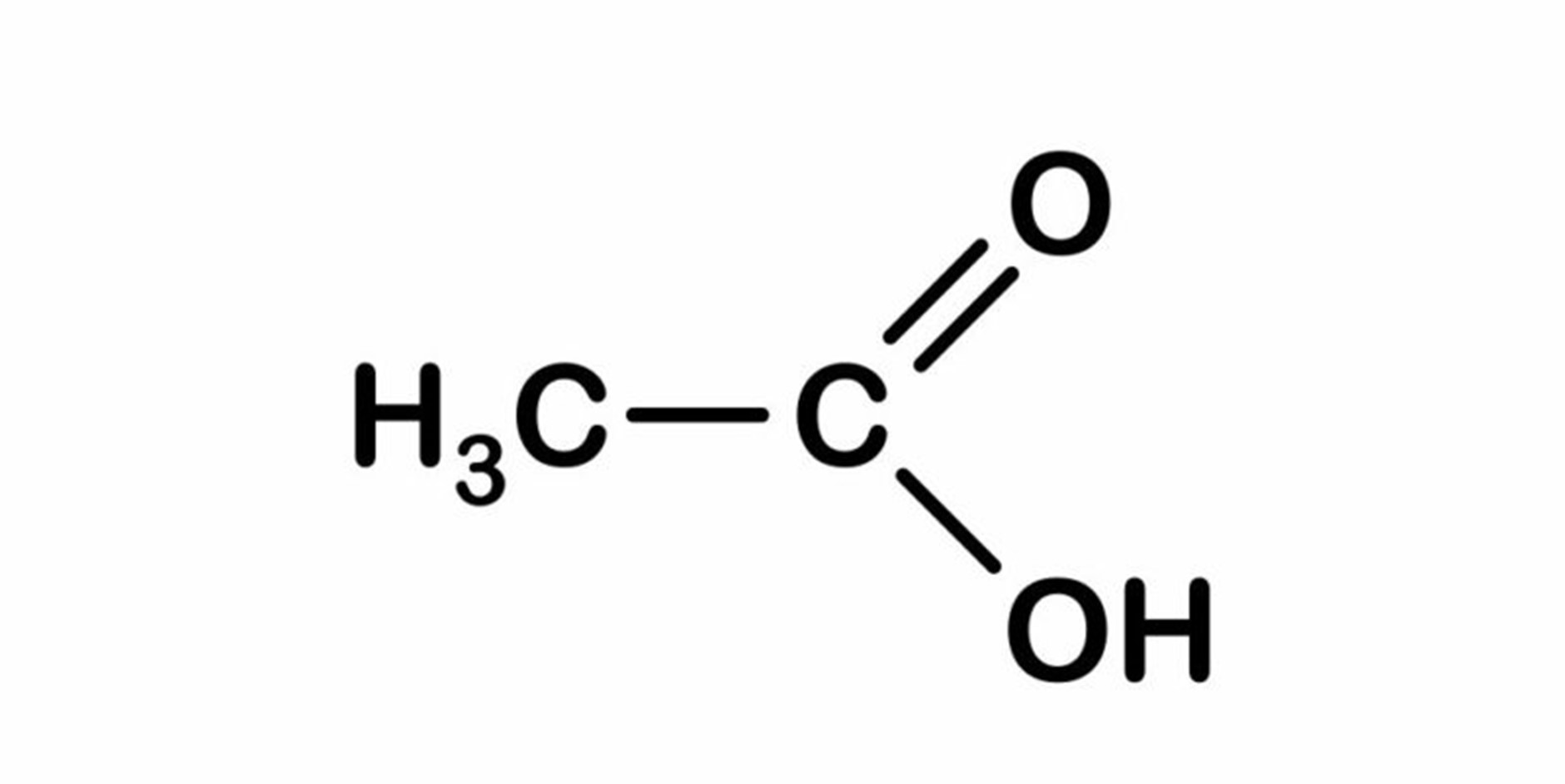
O ácido acético tem a fórmula química C 2 H 4 O 2 e a fórmula semi-desenvolvida CH 3 COOH. Daí se segue que é um grupo metil (CH3-) ligado por uma ligação simples de um átomo de carbono a um grupo carboxila (-COOH).
Solubilidade de ácido acético

O ácido acético é uma substância bastante polar porque tem um grupo polar (-COOH), embora também tenha um certo caráter apolar devido ao seu grupo (-CH3). Devido à presença de ambos os grupos em sua estrutura, é uma substância solúvel em água (solvente polar) , mas também é solúvel em muitas substâncias orgânicas menos polares.
Peso molecular do ácido acético
- Peso molecular . O ácido acético tem um peso molecular de 60,05 g / mol.
- Densidade . A densidade do ácido acético é 1049 kg / m3.
- Aparência . Pode ser um líquido transparente com forte odor de vinagre e gosto ácido, ou um sólido incolor na forma de pequenos cristais regulares.
Vinagre e ácido acético

O vinagre contém 3% a 5% de ácido acético dissolvido em água , junto com pequenas quantidades de ácido tartárico (C 4 H 6 O 6 ) e ácido cítrico (C 6 H 8 O 7 ).
Foi descoberto pela primeira vez na vinificação desde que os barris mal guardados, nos quais o ar e o oxigênio eram filtrados, passaram pelo processo de fermentação da bactéria Mycoderma aceti , que transforma o álcool etílico em vinagre. Foi dito então que o vinho estava “picado”.
O vinagre, no entanto, é uma parte importante da gastronomia humana e é produzido a partir de diferentes fontes: maçãs, uvas ou álcoois artificiais.
É indispensável no preparo de pickles, ceviche, pickles ou como tempero de saladas. Também é utilizado na preservação de alimentos , pois retarda os processos de decomposição da matéria orgânica.
Propriedades do ácido acético
O ácido acético é um ácido bastante fraco , apesar de ser inflamável e corrosivo ao mesmo tempo, além de uma substância higroscópica (que absorve água da umidade do ambiente).
Em altas concentrações, pode, portanto, irritar a pele, os olhos ou as membranas mucosas , tanto por inalação quanto por deglutição. É um ácido frequentemente secretado por seres vivos , como metabólito e substrato para as enzimas acetiltransferases.
Seu ponto de ebulição é 118 ° C, enquanto seu ponto de fusão é 17 ° C.
Ácido acético glacial

O ácido acético glacial é o resultado do congelamento do ácido acético , no qual a água que faz parte do composto forma cristais facilmente removíveis do composto. Uma vez que os cristais de água foram separados dos cristais de ácido acético, o ácido retorna ao estado líquido.
Assim, quando falamos em ácido acético glacial, nos referimos ao ácido acético anidro , ou seja, sem água.
Perigo de ácido acético
De modo geral, o ácido acético com o qual você entra em contato no vinagre e em outras soluções é encontrado em concentrações tão baixas que não é perigoso .
No entanto, em altas concentrações, é um ácido irritante capaz de causar queimaduras na pele , lesões permanentes nos olhos e irritação da mucosa.
Não é um composto particularmente inflamável , mas em soluções maiores que 25%, seus gases podem ser corrosivos e perigosos para a vida humana e animal, por isso é manuseado em uma coifa.
Obtenção de ácido acético
Algumas das principais formas de se obter ácido acético são por meio das seguintes reações:
- Carbonilação de metanol . Reação entre metanol e monóxido de carbono resultando em ácido acético.
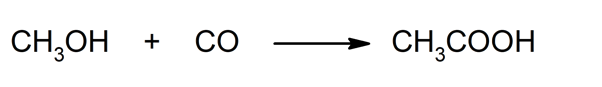
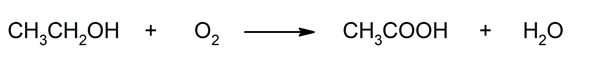
- Oxidação de etileno . O etileno é oxidado usando um metal como catalisador, paládio (Pd) neste caso.

- Fermentação oxidativa . Na presença de oxigênio, as bactérias do gênero Acetobacter podem produzir ácido acético a partir de certos compostos alcoólicos.
Aplicações de ácido acético

O ácido acético tem inúmeras aplicações em diferentes indústrias humanas, tais como:
- É utilizado como aditivo no controle da traça da cera (doença chamada galeriose) na apicultura.
- É um componente importante (formando sais ou ésteres) para fazer náilon, rayon, celofane e outros filmes sintéticos.
- É usado na fixação de substâncias para a preservação de tecidos orgânicos em laboratórios (como o formaldeído).
- É usado em produtos químicos para revelação fotográfica.
- É usado como um corante para revelar lesões do Vírus do Papilomavírus Humano (HPV) na medicina.
- É um componente comum em produtos de limpeza comerciais e removedores de manchas.
- Tem muitos usos culinários como vinagre: para lavar verduras e legumes, como tempero, etc.
Pode te ajudar: Ácido clorídrico